W. HASIBEDER
WO LIEGT DER „OPTIMALE TRANSFUSIONSTRIGGER“ FÜR PATIENT:INNEN MIT AKUTEN HIRNSCHÄDIGUNGEN
Für die meisten kritisch Kranken zeigen zahlreiche Studien, dass eine Anämie bis zirka 7g% als noch sicher angesehen wird. Eine Ausnahme von dieser Beobachtung haben wir in den letzten Literaturbesprechungen (5/2024) gezeigt – beim akuten Myokardinfarkt und Anämie liegt der „optimale Transfusionstrigger“ bei zirka 9g%, also wesentlich höher. In den Studien zur Transfusion kritisch Kranker sind Patient:innen mit akuten Hirnschäden meist unterrepräsentiert. Akute Hirnschädigungen gehen häufig mit einer Störung der Blutfluss Autoregulation und einer deutlichen Störung der Bluthirnschranke, Ödembildung und Veränderungen von Diffusionsstrecken sowie Kompression von Kapillaren und Venulen einher. Dies kann zu einer eingeschränkten Adaptationsfähigkeit bei akuter Anämie führen.
In einer neuen Multizenterstudie wurden 850 Patient:innen mit akuter Hirnschädigung (traumatisch; Aneurysmablutung; intrazerebrale Blutung), einem Hb < 9g% innerhalb der ersten 10 Tage nach Krankenhausaufnahme und einem erwarteten Intensivstationsaufenthalt > 72 Stunden in 2 Gruppen randomisiert:
- Eine liberale Transfusionsgruppe (LIB): Hier wurde bei Hb-Werten < 9g% sofort transfundiert
- Eine restriktive Transfusionsgruppe (RES): Hier wurde bei Hb-Werten <7g% transfundiert
Der primäre Outcomeparameter war das neurologische Outcome gemessen als Extended Glasgow Coma Score (Tabelle 1) gemessen bis zum 180 Tag
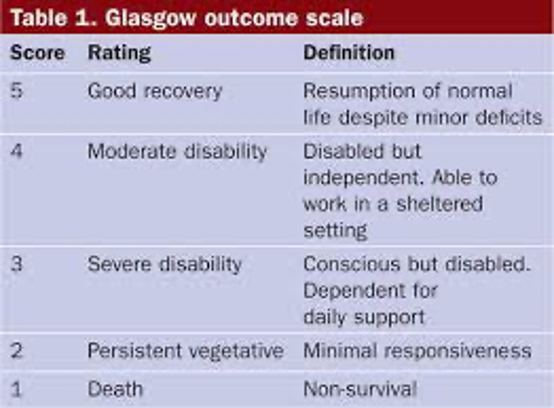
Das mittlere Patient:innen Alter lag bei 51 Jahren. Patient:innen in der LIB-Gruppe erhielten Median 2 (IQR: 1-3) Erykonzentrate, in der RES-Gruppe 0 (IQR: 0-1) EK während des Aufenthaltes. Nach 180 Tagen zeigten 62,6% in der LIB-Gruppe ein schlechtes neurologisches Outcome (EGCS: 1-3), während in der RES-Gruppe 72,6% der Patient:innen ein schlechtes neurologisches Outcome (EGCS: 4-5) aufwiesen. Die 28 Tage Mortalität war in den beiden Gruppen ähnlich (LIB: 8,8%; RES 13,5%; ns).
FAZIT für die Praxis: Ich denke wir sollten ähnlich wie beim anämischen Patienten/der Patientin mit akutem Myokardinfarkt unseren Transfusionstrigger bei schweren, akuten Hirnschädigungen erhöhen. Die Studie zeigt wieder einmal, dass eine „Kochbuchmedizin“ („one size fits all!“) keine Lösung für komplexe medizinische Probleme darstellt. Ich bin schon gespannt auf eine Untersuchung über den „optimalen“ Transfusionstrigger nach hypoxischen Hirnschäden, z.B. im Rahmen von Herzkreislaufstillstand und Reanimation.
Literatur:
Taccone FS, Bittencourt CR, MØller K, et al. Restrictive vs liberal transfusion strategy in patients with acute brain injury: the TRAIN randomized clinical trial. JAMA 2024; 332: 1623-1633
SOLLTE MAN HOCH RISIKOPATIENT:INNEN MIT HÜFTGELENKS-NAHEN FRAKTUREN SCHNELLER OPERIEREN?
Ältere oftmals vorerkrankte Patient:innen mit Hüftgelenks-nahen Frakturen haben ein signifikant erhöhtes Risiko, postoperativ kardiovaskuläre Komplikationen wie z.B. einen akuten Herzinfarkt oder Schlaganfall zu erleiden und zu Versterben. Leider wird immer noch wichtige Zeit für präoperative Abklärung oder Abwarten, wegen vorbestehender Antikoagulation, verschwendet. Dieses Vorgehen wird durch keinerlei wissenschaftliche Daten unterstützt! Derzeit gilt, dass das ideale Zeitfenster zur Versorgung Hüftgelenks-naher Frakturen bei älteren Patient:innen bei 24h bis maximal 48h liegt.
In „HIP ATTACK trial“ wurden 3000 ältere Patient:innen mit Hüftgelenks-nahen Frakturen randomisiert und entweder sehr rasch, innerhalb einer Medianzeit von 6 Stunden (ATTACK Patient:innen) oder, wie üblich innerhalb eines medianen Zeitintervalls von 24 Stunden, operiert. Es handelte sich bei allen Verletzungen um „niedrig-Energie“ Traumata – z.B. Sturz beim Gehen im Haus oder der Wohnung. Der primäre Outcomeparameter war der Tod beziehungsweise kardiovaskuläre Komplikationen innerhalb der ersten 90 Tage nach dem Trauma. Bei der Auswertung aller Patient:innen wurden keine wesentlichen Unterschiede in der 90 Tage Morbidität oder Mortalität gefunden. Wenn man hingegen nur jene Patient:innen betrachtet, die bereits mit erhöhtem Troponin T-Konzentrationen bei Aufnahme imponierten (23% aus 1392 Patient:innen) änderten sich die Ergebnisse signifikant:
- Patient:innen mit erhöhtem Troponin T bei Aufnahme zeigen eine deutliche Mortalitätssenkung durch frühzeitige, operative Osteosynthese in den ersten 6 Stunden. Die 90 Tage Mortalität sank von 23% auf 10%. Das entspricht einer „number needed to treat“ von 8!!
- Postoperative kardiovaskuläre Komplikationen, wie ein nicht tödlicher akuter Myokardinfarkt, eine dekompensierte Herzinsuffizienz oder Schlaganfälle bis zum 90 Tag traten in den „ATTACK“ Patientinnen signifikant weniger häufig auf (14% versus 30%)
FAZIT für die Praxis: Bei älteren Patient:innen mit Hüftgelenks-nahen Frakturen wird empfohlen bereits bei der Aufnahme das Troponin T zu bestimmen! Patient:innen mit erhöhten Werten profitieren signifikant von einer Frühosteosynthese innerhalb der ersten 6 Stunden (Medianwert)! Das bedeutet, dass Patient:innen mit Myokardschaden und Hüftfraktur von einer raschen Behebung des „pathophysiologischen“ Stresses, den diese Frakturen verursachen, profitieren. Dieser pathophysiologische Stress erklärt sich durch Schmerz, Inflammation, Hypovolämie und Ischämie durch Blutverluste in die Muskulatur und Dehydratation. Hoch-Risiko Patient:innen die erst nach 24h operativ stabilisiert werden haben eine doppelt so hohe 90 Tage Mortalität. Bei Patient:innen mit nicht erhöhten Herzmarkern kann und sollte eine Osteosynthese wie üblich, innerhalb von 24 Stunden (Medianwert) erfolgen.
Literatur:
Mattesi L, Noailles T, Rosencher N, et al. Discontinuation of Plavix for hip fracture surgery. A systematic review of the literature. Orthop traumatol Surg Res 2016; 102: 1097-1101
Wang J, Nilssen P, Stone J, et al. Expedited surgery does not increase transfusion rates for patients with geriatric hip fracture taking factor Xa inhibitors. OTA Int 2023; 22: e292
Mentsoudis SG. Preoperative echocardiography in hip fracture patients: a waste of time or good practice? Anaest Analg 2019; 128: 207-208
Pincus D, Ravi B, Wasserstein D, et al. Association between wait time and 30 days mortality in adults undergoing hip fracture surgery. JAMA 2017; 318: 1994-2003
Borges FK, Guerra-Farfan E, Bhandari M. Myocardial injury in patients with hip fracture: A HIP ATTACK randomized trial substudy. J Bone Joint Surg Am 2014; 108: 2303-2312
Cornell C. Patients presenting with myocardial injury with hip fracture have greater survival with rapid surgical care. J Bone Joint Surg Am 2024; doi: 10.2106/JBJS.24.00583
MÜSSEN ODER SOLLEN WIR AUF ERHÖHTE BLUTDRUCKWERTE BEI HOSPITALISIERTEN PATIENT:INNEN IMMER REAGIEREN?
Vor allem jüngeren Kolleg:innen ist es wichtig möglichst jede physiologische Variable eines Patienten/eine Patientin in einem „Normbereich“ zuhalten. Das betrifft auch den Blutdruck! Bei niederen Blutdruck gibt es mittlerweile, sowohl im perioperativen als auch im intensivmedizinischen Setting genügen Beweise, dass Hypotonie sowohl kardiale, zerebrale als auch renale Komplikationen verursacht und unbedingt rasch behandelt werden sollte. Aber was ist mit hypertensiven Phasen sofern sie nicht durch Schmerz- oder Stresserlebnisse verursacht werden?
In einer großen retrospektiven Untersuchung in amerikanischen Veteranenkrankenhäusern (n=130.000 nicht chirurgische Patient:innen; mittleres Alter 71+11 Jahre) wurden die Effekte von antihypertensiver Akuttherapie bei systolischen Blutdruckwerten > 140mmHg auf den weiteren intrahospitalen Verlauf näher untersucht. Die Patient:innen mussten mindestens 3 Tage stationär im jeweiligen Krankenhaus, auf einer nicht-chirurgischen Normalstation aufgenommen sein und zumindest 1 Blutdruckmedikament in den ersten 24 Stunden nach der Aufnahme erhalten haben. Primärer Outcome Parameter war das Auftreten einer akuten Nierenschädigung während des Krankenhausaufenthaltes. Weitere Outcome Parameter waren ein mindestens 25% Blutdruckabfall innerhalb der ersten 3 Stunden nach Gabe einer antihypertensiven Therapie sowie, als zusammengefasster Outcome Parameter, das Auftreten eines akuten Myokardinfarkts, eines Schlaganfalls oder das Versterben während des Aufenthaltes.
28.526 Patient:innen (21%) erhielten eine antihypertensive Therapie, außerhalb ihrer chronischen Vormedikation, zur Normalisierung hypertensiver Blutdruckwerte. Eine medikamentöse Korrektur plötzlich auftretender Blutdruckspitzen war mit erhöhtem Risiko für akute Nierenschäden (RR 1,23; CI: 1,18-1,29) assoziiert. Ebenso war das Risiko für unerwartete Hypotension (RR 1,5; CI: 1,39-1,62), sowie dem Auftreten von Tod, Herzinfarkt und Schlaganfall (RR 1,69; CI: 1,49-1,92) signifikant erhöht.
FAZIT für die Praxis: Plötzliche, asymptomatische hypertensive Blutdruckwerte sollten beobachtet, aber nicht sofort therapiert werden. Ein akuter, medikamentöser Eingriff in die Herzkreislaufregulation kann zu signifikanter Morbidität führen. Auch wenn diese Studie im konservativen Therapieumfeld stattgefunden hat, würde ich spekulieren, dass die Ergebnisse auch für den perioperativen und intensivmedizinischen Bereich Bedeutung haben. Allerdings gibt es bei uns zahlreiche zusätzliche Ursachen für hypertensive Blutdruckwerte. Schmerzen und psychischer Stress sind die häufigsten Ursachen für Blutdruckentgleisungen auf der Aufwach- und Intensivstation. Beides ist schlecht für unsere Patient:innen und gehört aggressiv behandelt! Allerdings sehen wir auch Patient:innen, die angeben schmerzfrei und angstfrei zu sein. Bei dieser Gruppe sollten hypertensive Phasen zunächst beobachtet und erst nach reiflicher Überlegung vorsichtig therapiert werden.
PERMISSIVE HYPOTENSION IM VASODILATORISCHEN SCHOCK – BESSER ALS NORMOTENSION?
Im vasodilatorischen Schock und insbesondere im septischen Schock sind steigende Katecholamindosierungen mit zunehmenden kardiovaskulären Risiken verbunden. Katecholamintoxizität führt zu Tachyarrythmien, pulmonaler Hypertension und Myokardischämien bis hin zum tödlichen Herzinfarkt. Wir konnten in einer Autopsie Studie, an Herzen im septischen Schock verstorbener Patient:innen, typische Zeichen der Katecholamintoxizität nachweisen. Ein Tod von Myokardzellen in maximaler Kontraktion führt zum typischen Bilden der „contraction band necrosis“. Katecholamintoxizität zeigt sich auch in einer ausgeprägten Inflammation des Myokards mit Lymphozyteninfiltration und Myokardödem.
In einer Metaanalyse von 3 bereits publizierten, randomisierten Studien (SEPSISPAM, OVATION Pilot Trial, 65-Trial) wurden die Effekte einer kontrollierten Hypotension (niedrige MAP Gruppe; nMAP: MAP 60-70mmHg) versus einer höheren MAP-Therapie (hMAP: MAP 70-85mmHg) auf die 90 Tage Mortalität untersucht. Insgesamt wurden 3352 Patient:innen aus 103 Krankenhäusern in die Metaanalyse inkludiert. Patienten der nMAP Gruppe hatten zeigten eine nicht signifikante Reduktion der Mortalität (-2,6%) im Vergleich mit der hMAP Gruppe.
Im 65-Trial wurden in der nMAP Gruppe 1221 und in der hMAP Gruppe 1242 Patient:innen (Mittleres Alter 75,3 + 6,6 Jahre) inkludiert. Patient:innen in den nMAP Gruppe benötigten weniger und kürzer Vasopressoren. Die 90 Tage Mortalität war ebenfalls nicht signifikant (41% versus 43,8%; -2,85%) geringer als in der hMAP Gruppe. Auch in anderen Outcomeparameter wie z.B. Notwendigkeit zur vv. Hämofiltration, Intensivaufenthaltstage, Hospitalsaufenthaltstage, Überleben nach einem Jahr, zunehmende kognitive Dysfunktion fanden sich keine signifikanten Gruppenunterschiede. In einer Subgruppenanalyse zeigte sich aber, dass Patient:innen mit vorbestehender chronischer Hypertension in der nMAP-Gruppe einen signifikanten Überlebensvorteil hatten (90 Tage Mortalität: 38,2% versus 44,3%; p< 0,047).
FAZIT für die Praxis: Unser Therapieziel für den MAP im septischen Schock war immer ein MAP zwischen 60mmHg und 70mmHg. Bei Patient:innen mit zunehmenden Vasopressorbedarf und Zeichen von Katecholamintoxizität tolerieren wir auch MAP Werte von 55mmHg bis 60mmHg ohne an der „Vasopressorschraube“ etwas zu erhöhen. In der Regel greifen, nach erfolgreicher Herdsanierung und Zugabe von Hydrocortison in Stressdosen, die Katecholamine nach einigen Stunden, durch zunehmende Rezeptorexpression an glatten Muskelzellen der Gefäßmuskulatur und die Katecholaminzufuhr kann reduziert werden. Selbstverständlich setzten wir auch frühzeitig Arginin -Vasopressin zur Blutdruckstabilisierung ein. Voraussetzung für eine erfolgreiche Katecholamin- und Vasopressorentherapie ist jedoch immer die vorherige Herstellung von Normovolämie. Im 65-Trial erscheint mit die 90 Tage Mortalität, mit > 40% extrem hoch zu sein. In einer Tabelle ist die Flüssigkeitszufuhr in den ersten 24 Stunden mit zirka 1250ml angegeben und das obwohl die Mehrzahl hypotensiver Patient:innen im septischen Schock war. Man kann sich des Eindruckes nicht erwehren, dass in dieser Studie möglicherweise eine Mehrzahl der Patient:innen nicht adäquat flüssigkeitstherapiert waren.
Literatur:
Dünser MW, Hasibeder WR. Sympathetic overstimulation during critical illness: adverse effects of adrenergic stress. J Intensive Care Med 2009; 24: 293-316
Schmittinger CA, Dünser MW, Torgersen C, et al. Histologic pathologies in the myocardium in septic shock: a prospective observational study. Shock 2013; 39: 329-335
Angriman F, Momenzade N, Adhikari NJ, et al. Blood pressure targets for adults with vasodilatory shock – an individual patient data meta-analysis. NEJM Evidence 2025; doi: 10.1056/EVIDoa2400359
Mouncey PR, Richards-Belle A, Thomas K, et al. Reduced exposute to vasopressors through permissive hypotension to reduce mortality in critically ill people aged 65 and over: the 65 RCT. Health Technology Assessment 2021; doi: 10.3310/hta25140
IST EINE MODERATE BLUTZUCKERFÜHRUNG BEI ÄLTEREN PATIENT:INNEN MIT DM TYP II MIT VERMEHRTEN INFEKTIONEN VERBUNDEN?
Ein intensives Behandlungsschema mit exakter Blutzuckerführung ist bei älteren Patient:innen häufig mit Komplikationen, wie z.B. Hypoglykämien, vergesellschaftet und von zu strenger Blutzucker Einstellung wird in klinischen Guidelines eher abgeraten. Eine mögliche Gefahr einer lockeren Blutzuckerführung sind Infektionen insbesondere der Haut, der Weichteile und der Knochen.
In einer großen retrospektiven Datenanalyse (n=103.242) wurden Patient:innen > 65 Jahre mit DM Typ 2 in 3 Gruppen, anhand ihrer HbA1c Spiegel, eingeteilt und im weiteren Verlauf wurden Infektionen des Respirationstrakts, des Genitourethraltraktes, der Haut, Weichteile, Knochen sowie das Syndrom der Sepsis erfasst. Insgesamt wurden 3,6% aller Patient:innen in den folgenden Monaten wegen Infektionen hospitalisiert. Patient:innen mit HbA1c Konzentrationen von 6%-6,9% zeigten keine signifikanten Unterschiede in der Inzidenz von Infektionen und Sepsis verglichen mit einer HbA1c (7%-7,9%) Gruppe. Allerdings traten in der HbA1c (8%-9%) Gruppe Infektionen mit Krankenhausaufnahmen signifikant häufiger auf (RR 1,33; CI: 1,05-1,69). Von der Art der Infektionen traten vor allem Haut-, Weichteil- und Knocheninfektionen gehäuft auf!
FAZIT für die Praxis: Es geht hier weniger um Akuttherapie, wie wir sie perioperativ oder auf der Intensivstation durchführen. Aber auch im perioperativen intensivmedizinischen Bereich hat letztlich die strikte Blutzuckerführung (80mg%-110mg%) gegenüber moderateren Zielwerten (bis 160mg%) keine Vorteile gebracht. Im Gegenteil gefährliche Hypoglykämien traten bei strenger BZ-Kontrolle signifikant häufiger auf. Was für unser Fach vielleicht interessant ist, ist die Tatsache dass bei älteren Patient:innen mit DM Typ 2 und moderater BZ-Führung (HbA1c 7% bis 8%) kein erhöhtes Infektionsrisiko verglichen mit Personen unter strikter BZ-Kontrolle besteht.
Literatur:
Lipska KJ, Gillam LK, Lee C, et al. Risk of infection in older adults with type 2 diabetes with relaxed glycemic control. Diabetes Care 2024; 47: 2258-2265
PARACENTESE BEI HOSPITALISIERTEN PATIENT:INNEN MIT LEBERZIRRHOSE – EHER FRÜH ODER SPÄTER?
Hospitalisierte Patient:innen mit Leberzirrhose haben eine erhöhtes Risiko eine primäre, spontane bakterielle Peritonitis zu entwickeln. Ein großes Problem dabei ist, dass zirka 1/3 der Fälle oligo- bis asymptomatisch verlaufen. Deshalb wird in existierenden Richtlinien eine diagnostische Paracentese bei allen hospitalisierten Patient:innen mit Leberzirrhose und Aszites gefordert! Was völlig unklar ist, war der optimale Zeitpunkt der Paracentese und mikrobiologischen Untersuchung des Aszites.
In einer großen Metaanalyse an mehr als 78.000 hospitalisierten Patient:innen, die einer diagnostischen Paracentese unterzogen wurden zeigte sich, dass eine Paracentese innerhalb der ersten 12-24h nach Krankenhausaufnahme (n=45.533) verglichen mit einer Paracentese nach 24h (n=33.211) mit einem signifikant verbesserten Outcome einhergeht. Patient:innen mit früher diagnostischer Paracentese entwickelten signifikant weniger häufig ein akutes Nierenversagen (24% versus 35%; OR 0.62; CI: 0.42-0.92; p=0.02), waren im Mittel 5 Tage früher aus dem Krankenhaus entlassen und hatten eine geringere Krankenhausmortalität (7% versus 10%; OR 0,61; CI: 0.46-0.82; p< 0,001). Die Mortalitätsunterschiede waren größer, wenn eine diagnostische Parazentese innerhalb der ersten 12h nach Krankenhausaufnahme durchgeführt wurde.
FAZIT für die Praxis: Die Ergebnisse sind klar: Im Krankenhaus aufgenommene Patient:innen mit Leberzirrhose und Aszites sollten bereits innerhalb der ersten 12h bis maximal 24h nach Aufnahme einer diagnostischen Paracentese unterzogen werden. Ich denke es sollte möglich sein, z.B. in den zuständigen Ambulanzen oder der Notaufnahme, sofort diesen einfachen Eingriff durchzuführen um, bei Diagnose einer spontanen Peritonitis, rasch mit einer Antibiotika- und Albumintherapie beginnen zu können.
Literatur:
Biggins SW, Angeli P, Garcia-Tsao G, et al. Diagnosis, evaluation and management of ascites, spontanuous bacterial peritonitis and hepatorenal syndrome: 2021 practice guidance by the American Association for the study of Liver Diseases. Hepatology 2021; 74: 1014-1048
Beran A, Mohamed MFH, Vargas A, et al. Early diagnostic paracentesis improves outcome of hospitalized patients with cirrhosis and ascites: a systematic review and meta-analysis. Am J Gastroenterol 2024; 119: 2259-2266
WIE SOLL EINE SCHWERE HYPONATRIÄMIE KORRIGIERT WERDEN?
Um eine zentrale pontine Myelinolyse (CPM), eine osmotisch bedingte Demyelinisierung von Nervenfasern vor allem in der Pons-Region, möglichst zu vermeiden empfehlen internationale Richtlinien eine langsame Korrektur einer vorbestehenden schweren Hyponatriämie. Die Korrektur des Serum Natriumspiegels sollte maximal 10-12 mmol/l in den ersten 24 Stunden und < 18 mmol/l in den ersten 48h Therapie betragen.
Allerdings beruhen diese Empfehlungen auf mangelhaften Studien und jüngste Publikationen weisen darauf hin, dass eine schnellere Korrektur einer schweren Hyponatriämie mit keinem erhöhten Risiko einer CPM einhergeht.
In einer großen Metaanalyse von 16 Studien (12.000 Patient:innen; mittleres Alter 68 Jahre) wurden Korrekturraten einer schweren Hyponatriämie (Na+ < 120-125mmol/l) wie folgt eingeteilt:
- Sehr schnelle Korrektur: > 12 mmol/l und 24h
- Schnelle Korrektur: > 8 bis 10 mmol/l und 24h
- Langsame Korrektur: 6-10 mmol/l und 24h
- Sehr langsame Korrektur: <4 bis 6mmol/l und 24h
Verglichen mit einer langsamen oder sehr langsamen Korrektur einer Hyponatriämie war die schnelle und sehr schnelle Korrektur mit weniger Todesfällen im Krankenhaus und bis zum 30. Tag nach Behandlungsbeginn assoziiert. Die Krankenhausaufenthaltsdauer war bei schneller Korrektur um 1-3 Tage kürzer. Die Inzidenz des Auftretens einer CPM war in Gruppenvergleich statistisch nicht signifikant unterschiedlich (sehr schnell 0,3%; schnell 0,5%, langsam 0,2%, sehr langsam < 0,1%)
FAZIT für die Praxis: Auch wenn es sich bei den eingeschlossenen Studien um retrospektive Fallanalysen handelt kann mit großer Sicherheit festgestellt werden, dass eine Korrekturgeschwindigkeit einer Hyponatriämie bis zu 12mmol/l und 24 Stunden zu keinem erhöhten Risiko neurologischer Schäden führt.
Literatur:
Ayus JC, Moritz ML, Fuentes NA, et al. Correction rates and clinical outcomes in hospitalized adults with severe hyponatriemia. JAMA Intern Med 2025; 185: 38-51
Winawer NH. Correcting severe hyponatriemia: Don`t go too slow. NEJM Journal Watch. November 19; 2024
